生物钟是一个高度分层的内源性调节网络,其核心通过转录—翻译反馈环路维持并引导节律基因振荡,调控细胞和组织中内分泌与代谢的节律周期。尽管已知昼夜节律调控代谢过程及相关生理功能,但新证据表明代谢与昼夜节律存在密切的互相作用。针对特定功能性代谢物,可以为昼夜节律紊乱、病理性衰老开发新的疾病治疗策略。
2025年4月29日,Journal of Genetics and Genomics在线发表中国科学院遗传与发育生物学研究所税光厚研究组题为“The circadian clock at the intersection of metabolism and aging – emerging roles of metabolites”的综述文章,该综述总结了代谢物在昼夜节律与衰老进程中的重要作用,为治疗昼夜节律紊乱和延缓衰老提供了全新视角。该综述首先介绍了昼夜节律的概念和背景,并且通过轮班工人节律失调易患心血管疾病以及衰老相关疾病的临床数据表明昼夜节律、衰老和代谢存在紧密联系,进而探讨代谢与昼夜节律双向调节关系,提出代谢物作为“授时因子”可以起到改善节律失调、延缓衰老的作用。其次,该综述系统总结了以BMAL1/CLOCK为核心的生物钟分子机制,详细介绍了代谢物如葡萄糖、脂质和褪黑素的节律性维持生理稳态的功能。随后,该综述进一步阐述了限制饮食通过影响衰老相关通路包括mTOR、AMPK、PGC-1α等作用于节律基因调节代谢和衰老。该综述也系统总结了核心节律基因对代谢性疾病和衰老的具体影响,讨论了节律基因紊乱与代谢性疾病、加速衰老的联系。最后,该综述分析并展望了代谢物作为生物节律授时因子在改善节律、延缓衰老等方面的应用潜力。
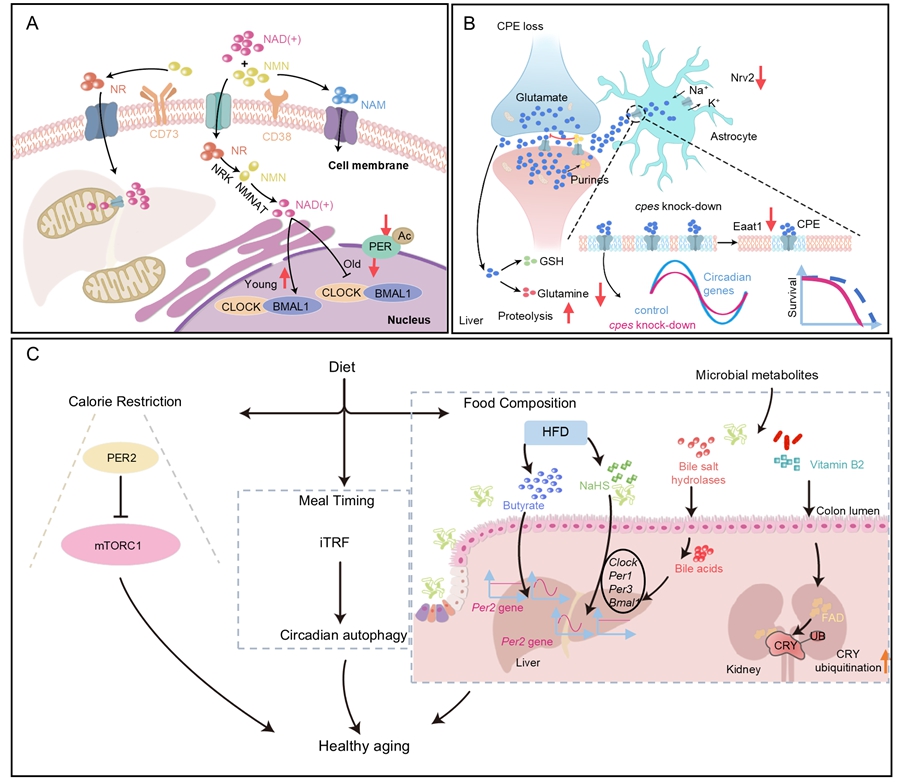
其中该综述重点强调代谢物不仅是生物钟调控的产物,更是驱动昼夜节律、延缓衰老的关键“授时因子”:脂质代谢物CPE(神经酰胺磷酸乙醇胺,哺乳动物中主要为鞘磷脂SM)通过维持神经胶质细胞膜微域功能,调控果蝇运动节律并显著影响寿命;而NAD+(烟酰胺腺嘌呤二核苷酸)水平随年龄下降会影响生物钟基因表达节律,补充其前体烟酰胺核苷可恢复老年小鼠的代谢节律并改善胰岛素抵抗;肠道微生物代谢物如丁酸盐和FAD(黄素腺嘌呤二核苷酸)通过肠道影响肝脏和肾脏生物钟蛋白降解和能量代谢,参与宿主昼夜节律的调控,影响健康衰老;Per2在卡路里限制期间抑制mTORC1活性延缓衰老;此外,在老年小鼠中进行限制性饮食恢复了肌肉中昼夜节律基因的节律性表达,使得肌肉信号传导和昼夜节律基因表达的幅度与年轻小鼠相当等。这些发现强调代谢物作为“授时因子”可以发挥驱动昼夜节律与延缓衰老的功能,未来通过精准调控代谢物节律(如补充NAD+前体、优化饮食时间或靶向微生物代谢物)或可成为改善生物钟紊乱、对抗衰老及相关疾病的全新策略,为治疗生物节律紊乱、健康老龄化开辟代谢干预新路径。
中国科学院遗传与发育生物学研究所在读博士生董月与Sin Man Lam博士为该论文共同第一作者,中国科学院遗传与发育生物学研究所税光厚研究员、陆军军医大学西南医院李旻典教授以及中国科学院生物物理研究所李岩研究员为共同通讯作者。相关工作得到中国科学院、广州国家实验室重大项目和国家自然科学基金资助。
图:代谢物作为昼夜节律“授时因子”发挥改善节律紊乱、延缓衰老的功能